Ecco cosa sono i metalli di transizione: un gruppo di elementi che colmano il divario tra due lati della tavola periodica. In questo articolo ci immergeremo nel meraviglioso mondo di questi metalli.
- Questo articolo è un'introduzione ai metalli di transizione nella chimica inorganica.
- Inizieremo definendo i metalli di transizione.
- Poi vedremo la loro posizione nella tavola periodica.
- Esamineremo le loro proprietà generali.
- Infine, esploreremo alcuni dei loro usi e applicazioni.
Cosa sono i metalli di transizione?
Gli scienziati a volte non sono d'accordo sull'esatta classificazione dei metalli di transizione. In effetti, esistono definizioni diverse.
Ma per il momento è necessario sapere quanto segue:
I metalli di transizione sono elementi che formano almeno uno ione stabile con un sottoguscio d parzialmente riempito di elettroni.
Si potrebbe pensare che questa definizione comprenda tutti gli elementi del blocco d della tavola periodica, ma in realtà non è così. Infatti, non tutti gli elementi del blocco d formano ioni stabili con sottogusci d incompleti. Esempi di elementi del blocco d che non sono metalli di transizione sono lo scandio (Sc) e lo zinco (Zn). Vedremo più avanti il perché.
I metalli di transizione sono rappresentati nella tavola periodica qui sotto. Qui sono evidenziati in blu.
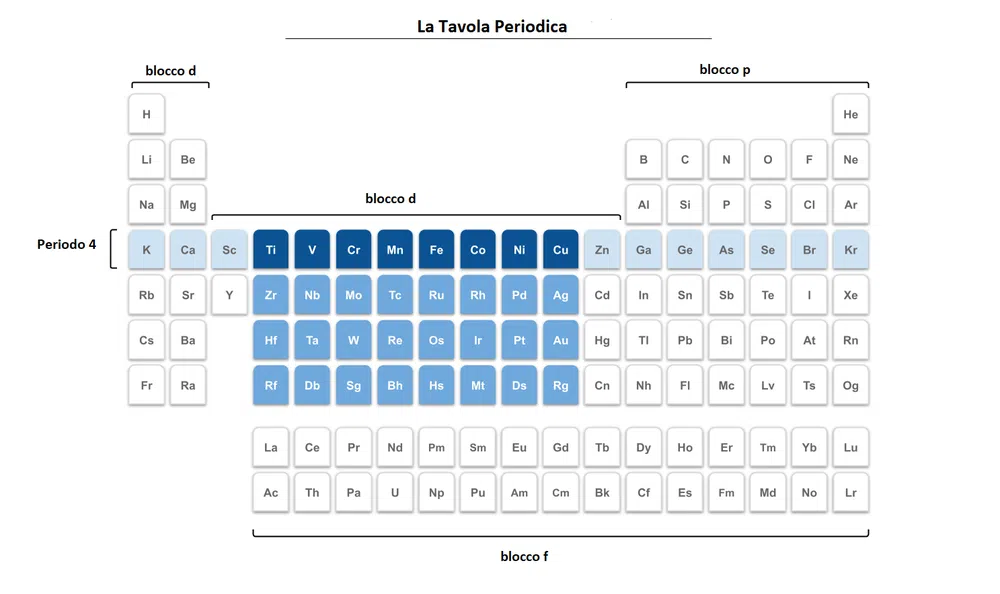
Figura 1. Tavola periodica degli elementi con evidenziati i metalli di transizione.
La IUPAC (Unione Internazionale di Chimica Pura e Applicata) ha una definizione leggermente diversa di metallo di transizione. Concordano sul fatto che un metallo di transizione sia un elemento che forma almeno uno ione stabile con un sottoguscio d parzialmente riempito di elettroni, ma dicono anche che i metalli di transizione possono essere elementi i cui atomi hanno una sottoguscio d parzialmente riempito. Questa definizione significa che lo scandio e lo zinco sono di fatto metalli di transizione.
Si possono anche vedere i lantanidi, elementi con numero atomico 57-71, e gli attinidi, con numero atomico 89-103, definiti metalli di transizione interni. Per questo articolo, però, ci atterremo alla prima definizione che abbiamo appreso: solo gli elementi evidenziati in blu qui sopra.
Metalli di transizione nella tavola periodica
Come abbiamo mostrato sopra, i metalli di transizione si trovano al centro del blocco d della tavola periodica.
Il blocco d è una sezione della tavola periodica. Il sottoguscio a più alta energia che si trova negli elementi del blocco d è sempre un sottoguscio d. Il blocco d si trova tra il blocco s e il blocco p e costituisce un collegamento tra i due.
Più precisamente, i metalli di transizione si trovano nei gruppi 3-12 e nei periodi 4-7, ma questo non è importante: tutto ciò che conta è che si possano trovare nella tavola periodica.
Configurazione elettronica dei metalli di transizione
Inizieremo con la loro configurazione elettronica come atomi, per poi vedere come questa cambia quando si formano gli ioni. Questo ci aiuterà anche a spiegare perché alcuni membri del blocco d non sono classificati come metalli di transizione.
Questa sezione probabilmente non avrà molto senso se non si è letto Gusci di elettroni e Configurazione degli elettroni. Si consiglia di leggerli prima per imparare le basi dei gusci di elettroni, dei sottogusci, degli orbitali e delle regole di riempimento.
Configurazione elettronica degli elementi di transizione
Come abbiamo detto, tutti i metalli di transizione si trovano nel blocco d della tavola periodica. Ciò significa che i loro elettroni di valenza si trovano tutti in un sottoguscio d.
Occorre ricordare che gli elettroni si trovano in gusci. Questi sono suddivisi in sottogusci. Esistono quattro tipi diversi di sottogusci di elettroni: i sottogusci s-, p-, d- e f-. La posizione di un elemento nella tavola periodica indica il sottoguscio di massima energia in cui si trovano i suoi elettroni. Il sottoguscio a più alta energia che si trova negli elementi del blocco p, ad esempio, è un sottoguscio p.
Man mano che ci si sposta nel periodo della tavola periodica, ogni metallo di transizione ha un elettrone in più rispetto a quello precedente. Questi elettroni riempiono gradualmente il sottoguscio d, ma ci sono alcune eccezioni. Diamo un'occhiata più da vicino, usando come esempio la prima fila di metalli di transizione (periodo 4). Di seguito abbiamo evidenziato il periodo.
 Figura 2. Tavola periodica con evidenziato il Periodo 4.
Figura 2. Tavola periodica con evidenziato il Periodo 4.
Diamo un'occhiata alle loro configurazioni elettroniche. Come nella tavola periodica, abbiamo evidenziato i metalli di transizione.
 Figura 3. La configurazione elettronica del periodo 4.
Figura 3. La configurazione elettronica del periodo 4.
I primi due elementi del periodo 4, il potassio (K) e il calcio (Ca), si trovano nel blocco s. I loro elettroni di valenza si trovano nel guscio secondario 4s e i loro gusci secondari 3d sono vuoti.
Ricorda che i sottogusci si riempiono in un certo ordine, dall'energia più bassa a quella più alta. Di solito segue lo schema dal numero più basso al numero più alto. Ad esempio, 2s si riempie prima di 3s. Tuttavia, 3d è un'anomalia: ha un'energia leggermente superiore a 4s e quindi si riempie dopo 4s. Questo è solo un altro esempio di una fastidiosa eccezione alle regole che devi imparare!
I 10 elementi successivi sono elementi del blocco d. Man mano che si procede nel periodo, gli elettroni vengono aggiunti al sottoguscio interno 3d, uno alla volta. Ad esempio, lo scandio (Sc) ha 21 elettroni e ha un solo elettrone nel suo sottoguscio 3d, il che gli conferisce la configurazione elettronica di [Ar] 3d1 4s2, mentre il titanio ha 22 elettroni e ha due elettroni nella sua sottoguscia 3d. Ciò gli conferisce la configurazione elettronica di [Ar] 3d2 4s2.
Ma, come abbiamo detto, questo schema di riempimento è bruscamente interrotto da due elementi: il cromo (Cr) e il rame (Cu). Entrambi hanno sottogusci 4s parzialmente riempiti. Perché questo fenomeno?
È perché i sottogusci 4s e 3d hanno livelli energetici molto simili. Poiché l'elettrone nel guscio secondario 4s non è accoppiato, non subisce alcuna repulsione elettrone-elettrone. Questo abbassa il suo stato energetico e compensa l'elettrone in più nel guscio secondario 3d, che ha un'energia leggermente superiore. Gli elettroni preferiscono trovarsi nello stato energetico più basso possibile. Si ritiene inoltre che avere un semiguscio 3d pieno, come nel caso del cromo, o un semiguscio 3d completamente pieno, nel caso del rame, aiuti a stabilizzare l'atomo.
 Figura 4. Configurazioni elettroniche previste e osservate di cromo e rame.
Figura 4. Configurazioni elettroniche previste e osservate di cromo e rame.
Configurazione elettronica dei metalli di transizione
Tutti i metalli di transizione formano cationi positivi perdendo elettroni.
Si ricorderà dalla Configurazione degli elettroni che, sebbene il sottogruppo 3d sia di livello energetico leggermente superiore al sottogruppo 4s, gli atomi perdono prima gli elettroni del sottogruppo 4s. Ciò significa che tutti i metalli di transizione hanno perso gli elettroni 4s prima degli elettroni 3d.
Prendiamo ad esempio il ferro (Fe). Forma comunemente ioni con cariche di 2+ o 3+. Il ferro ha la configurazione elettronica di [Ar] 3d6 4s2. Quando si forma uno ione 2+, esso perde innanzitutto i suoi elettroni 4s, assumendo la configurazione elettronica di [Ar] 3d6 4s0. Per formare uno ione 3+, deve perdere un altro elettrone. Poiché il sottogruppo 4s è ora vuoto, questo elettrone viene perso dal sottogruppo 3d, dando allo ione la configurazione elettronica di [Ar] 3d5 4s0.
 Figura 5. La configurazione elettronica del ferro, del ferro(II) e del ferro(III).
Figura 5. La configurazione elettronica del ferro, del ferro(II) e del ferro(III).
Perché gli elementi del blocco d non sono tutti metalli di transizione?
Questo perché non tutti formano ioni stabili con sottogusci d incompleti. Ad esempio, lo scandio (Sc) forma solo ioni 3+ in tutti i suoi composti, il che gli conferisce la configurazione elettronica di [Ar] 3d0 4s0. Il suo sottoguscio 3d è completamente vuoto, quindi non è un metallo di transizione. Allo stesso modo, lo zinco (Zn) forma solo ioni 2+ in tutti i suoi composti. Questi ioni hanno la configurazione elettronica di [Ar] 3d10 4s0. Il suo sottoguscio 3d è completamente pieno, quindi non è un metallo di transizione.
Proprietà dei metalli di transizione
I metalli di transizione hanno proprietà simili. Sono buoni conduttori di calore ed elettricità, sono duri e resistenti e hanno punti di fusione e di ebollizione elevati. Rispetto ai metalli del gruppo 1 e 2, sono anche relativamente poco reattivi. Questo li rende estremamente utili, ma ne parleremo nella prossima sezione. Per ora, analizziamo alcune delle loro altre proprietà caratteristiche. Ce ne sono quattro in particolare che è necessario conoscere quando si parla di metalli di transizione:
- I metalli di transizione formano ioni con più stati di ossidazione. Abbiamo già visto che il ferro forma ioni 2+ e 3+.
- Formano ioni complessi. Gli ioni complessi sono ioni legati ad altri ioni o molecole, detti ligandi, mediante legami covalenti dativi.
- Formano composti colorati. Ad esempio, il rame forma spesso soluzioni blu.
- Sono buoni catalizzatori, ovvero sostanze che aumentano la velocità di una reazione chimica senza essere consumate nel processo.
Esploreremo in dettaglio queste proprietà in Proprietà dei metalli di transizione.
Usi dei metalli di transizione
Grazie alle loro proprietà, i metalli di transizione hanno un'ampia varietà di usi. Li troviamo nell'elettronica, nei materiali da costruzione e in molti altri settori. Ecco alcune delle loro applicazioni più comuni:
L'alluminio è leggero e non tossico, quindi viene utilizzato non solo per la produzione di pezzi di automobili e aerei, ma anche per la fabbricazione di lattine e fogli per avvolgere gli alimenti.
Il ferro è utilizzato nei materiali da costruzione, ad esempio nei ponti, nelle navi e nelle strutture degli edifici. Ciò è dovuto alla sua elevata resistenza e al suo basso costo. Il ferro rappresenta infatti il 90% della produzione mondiale di metalli.
Il rame è utilizzato nei cavi elettrici grazie alla sua buona conducibilità elettrica.
Il titanio in polvere si trova nell'industria pirotecnica, ad esempio nei fuochi d'artificio, perché produce particelle luminose.
Il tungsteno è utilizzato nei filamenti delle lampadine e nei tubi a raggi X.
I metalli di transizione formano spesso leghe. Si tratta di composti formati da miscele di elementi, di cui almeno uno è un metallo. Le leghe sono generalmente più resistenti dei metalli puri. I metalli formano dei reticoli e nei metalli puri gli ioni metallici all'interno del reticolo sono tutti della stessa dimensione, quindi è facile che scivolino l'uno sull'altro.
Tuttavia, le leghe contengono ioni metallici di dimensioni diverse. Questi distorcono il reticolo e rendono più difficile lo scorrimento degli ioni gli uni sugli altri. Tra le leghe di metalli di transizione utili vi sono l'ottone (composto da rame e zinco), l'acciaio (composto da ferro e carbonio, un non metallo) e l'argento massiccio (composto da argento e un altro metallo, di solito rame).
Per ulteriori informazioni sui reticoli metallici, consultare la sezione Legami metallici.
Metalli di transizione - Punti chiave
I metalli di transizione sono elementi i cui atomi hanno un sottoguscio d parzialmente riempito o che formano almeno uno ione stabile con un sottoguscio d parzialmente riempito di elettroni.
I metalli di transizione si trovano nel blocco d della tavola periodica. Questo significa che il loro sottoguscio a più alta energia è sempre un sottoguscio d. Più precisamente, i metalli di transizione si trovano nei gruppi 3-12 e nei periodi 4-7.
I metalli di transizione si differenziano per il numero di elettroni presenti nei loro sottogusci d. Tuttavia, il rame e il cromo presentano configurazioni elettroniche leggermente diverse da quelle attese, a causa della somiglianza dei livelli energetici dei gusci 4s- e 3d.
Quando formano ioni, i metalli di transizione perdono gli elettroni 4s prima degli elettroni 3d.
I metalli di transizione sono duri e resistenti, hanno punti di fusione e di ebollizione elevati e sono relativamente poco reattivi.
I metalli di transizione formano anche ioni con stati di ossidazione multipli, formano ioni complessi, producono composti colorati e agiscono come catalizzatori.
I metalli di transizione sono utilizzati come materiali da costruzione e in elettronica. Inoltre, formano molte leghe diverse.