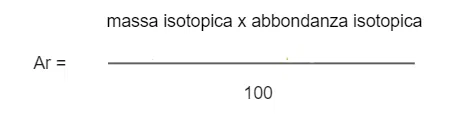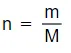- In questo articolo sulla quantità di sostanza, imparerai a conoscere la costante di Avogadro (NA o L) e a calcolare il numero di moli (n).
- Scoprirai anche la massa atomica relativa (Ar) e perché usiamo l'unità di massa atomica unificata (u).
- Parleremo della resa percentuale e del perché la resa effettiva è inferiore a quella teorica. Infine, imparerai l'equazione dei gas ideali e la teoria cinetica dei gas.
- Questo è un articolo riassuntivo; per saperne di più, dai un'occhiata gli argomenti collegati.
Che cos'è la quantità di sostanza?
La quantità di sostanza (n) indica il numero di particelle o entità elementari presenti in un campione. È anche chiamata quantità chimica.
Un'entità elementare è la più piccola quantità di una sostanza che può esistere. Le entità elementari possono essere atomi, molecole, ioni o elettroni.
Quando si parla di quantità di sostanza è necessario specificare quale entità elementare è coinvolta. Ad esempio, si consideri l'elemento ossigeno.
Si potrebbe pensare che l'entità elementare di una quantità di ossigeno sia l'atomo di ossigeno -O. Tuttavia, a temperatura e pressione standard due atomi di ossigeno si combinano in ossigeno molecolare O2. Ciò significa che l'entità elementare dell'ossigeno è O2.
Quando si parla di quantità di sostanza dei composti covalenti, si intende la loro formula molecolare. Per i composti ionici, invece, si intende la loro formula unitaria.
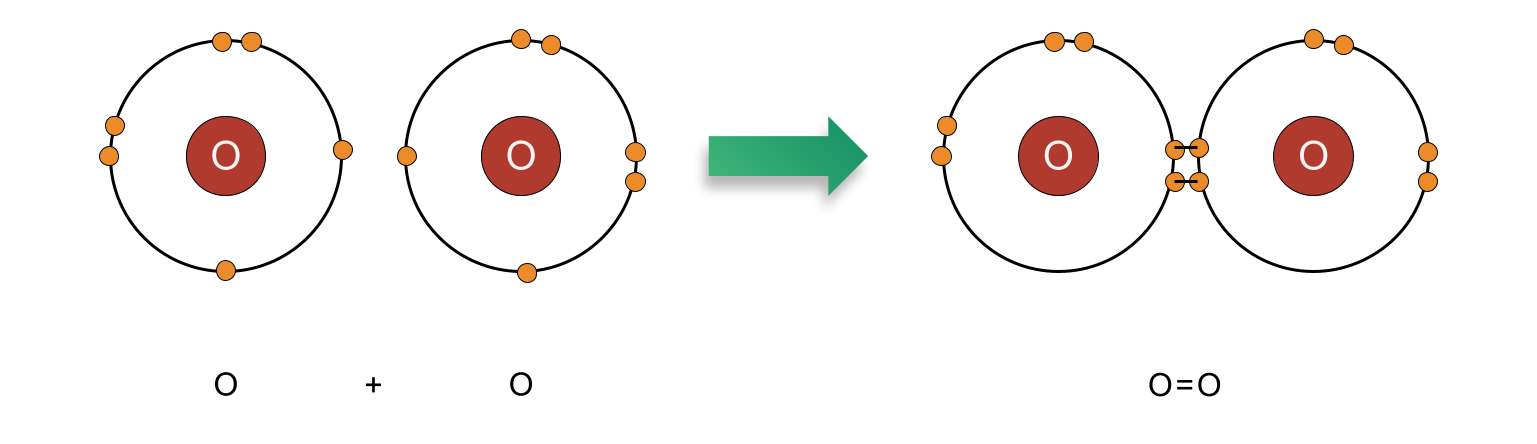
Figura 1. L'ossigeno è una particella biatomica. Esiste in coppia, quindi l'entità elementare dell'ossigeno è O
2.
Quantità di sostanza unità di misura
L'unità di misura della quantità di sostanza è la mole.
Che cos'è la mole?
Una mole chimica è un altro modo di indicare una quantità esatta. Proprio come diciamo "una dozzina" per indicare "dodici cose", una mole è "602 esilioni di cose", ovvero, 602'200'000'000'000'000'000'000! Lo scriviamo per abbreviare.
 Figura 2. Una gallina fa 602 esilioni di uova!
Figura 2. Una gallina fa 602 esilioni di uova!
Il numero è noto anche come costante di Avogadro (NA o L). Prende il nome da uno scienziato italiano chiamato Amedeo Avogadro. Egli scoprì che volumi uguali di gas contengono lo stesso numero di molecole a parità di condizioni. Gli scienziati hanno utilizzato questa scoperta per calcolare la costante di Avogadro.
La costante di Avogadro (L) è il numero esatto di atomi in 12 grammi di carbonio-12. Questo numero è 6.022x1023. Gli assegnamo l'unità mol-1 , che si legge "per mole".
La mole è l'unità SI per la quantità di sostanza.
Puoi trovare il numero di moli utilizzando la formula:

o
n: numero di moli
m: massa in grammi
M: massa molare (massa di una mole in grammi)
La quantità di entità elementari in una mole è pari al numero di atomi presenti in 12 g dell'isotopo carbonio-12.
Ciò significa che in 1 mole di qualsiasi sostanza ci sono esattamente 6.022 x 1023 entità elementari o la costante di Avogadro.
1 mole di una sostanza pesa 80 g e tu ne hai 10 g. Quante moli della sostanza hai?


Perchè la mole è importante?
La mole è essenziale quando parliamo di reazioni chimiche. Considera questa equazione:

Possiamo dire "ossigeno e idrogeno reagiscono per produrre acqua"
o
"Due molecole di idrogeno e una molecola di ossigeno reagiscono per produrre acqua" .
Hai notato che abbiamo bisogno di un numero di molecole di idrogeno due volte superiore a quello dell'ossigeno? Quindi, se avessimo 1 mole di idrogeno e 1 mole di ossigeno, avremmo lo stesso numero di molecole - la costante di Avogadro. Per essere sicuri di avere il doppio delle molecole di idrogeno, abbiamo bisogno del doppio delle moli di idrogeno.
Ciò significa che possiamo anche dire "2 moli di idrogeno reagiscono con 1 mole di ossigeno per produrre 2 moli di acqua".
La mole è utile perché consente di leggere le equazioni chimiche in base al numero di moli di ciascuna sostanza. In questo modo è possibile determinare le quantità esatte di sostanze che stanno reagendo.
La massa di una mole di una sostanza è uguale alla sua formula di massa.
Che cos'è la massa relativa?
Gli scienziati misurano la massa di un atomo confrontandola con 1/2 della massa di un atomo neutro di carbonio-12. Si tratta della cosiddetta massa relativa.
Esprimiamo la massa relativa facendo riferimento all'unità di massa atomica unificata (u o Dalton).
Un dalton (1u) equivale a 1/2 della massa di un atomo stabile di carbonio-12 o a 1.660539040(20) x 10-27 kg.
Tutti gli atomi vengono comparati con 1/2 della massa del carbonio-12 poichè è uguale a 1u.
u è l'unità di misura per la massa atomica. 1u è uguale a 1/2 della massa dell'atomo di carbonio-12.
Perchè utilizziamo la massa relativa?
Usiamo le masse relative perché gli atomi sono così piccoli che l'utilizzo dei loro pesi reali rende i calcoli difficili. Invece di usare la massa effettiva degli atomi nei problemi, gli scienziati confrontano tutti gli atomi con un atomo standard: il carbonio-12. Usano il carbonio-12 perché è un isotopo stabile e possono misurarlo con precisione. Usano il carbonio-12 perché è un isotopo stabile e possono misurarne la massa con precisione. Il carbonio-12 è un isotopo del carbonio con 6 protoni e 6 neutroni. Hanno scoperto che l'atomo di carbonio-12 pesa 6 x 10-23 grammi.
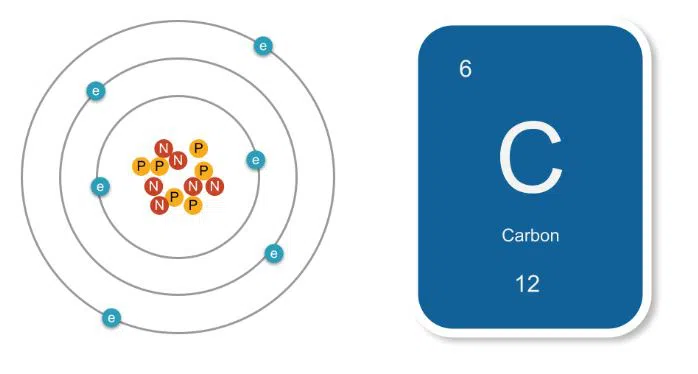
Figura 3. Il carbonio-12 è l'isotopo del carbonio più abbondante in natura. Massa = 6x10
-23 o
12 uGli scienziati hanno dato al carbonio-12 una massa di 12u perché trovavano più facile dire "il carbonio-12 pesa 12u". Confrontando il peso di tutti gli altri atomi con il carbonio-12 hanno scoperto che l'atomo di idrogeno pesa quanto 1/2 dell'atomo di carbonio-12. Quindi hanno dato all'idrogeno una massa relativa di 1u.
idrogeno = massa carbonio ÷ 12
=12u ÷ 12
=1u
Che cos'è la massa atomica relativa?
La massa atomica di un elemento varia da un isotopo all'altro. La cifra che vediamo per la massa atomica di un elemento sulla tavola periodica è la massa atomica relativa.
La massa atomica relativa (Ar) è la massa media di tutti gli isotopi di un elemento, pesata per l'abbondanza di ciascun isotopo sulla Terra.
Si può calcolare la massa atomica relativa utilizzando la formula:
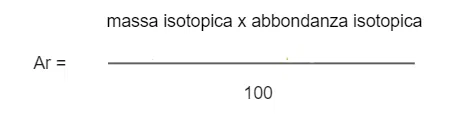
Che cos'è la massa molecolare relativa?
La media ponderata della massa di una molecola rispetto a 1/2 della massa di un atomo di carbonio-12 è chiamata massa molecolare relativa (Mr o RMM).
Che cos'è la resa percentuale?
Quando si confronta la quantità effettiva di prodotto ottenuto da una reazione chimica con la quantità che teoricamente si sarebbe potuta ottenere, si parla di resa percentuale.
La resa percentuale misura l'efficacia di una reazione chimica. Ci dice la quantità dei nostri reagenti (in termini percentuali) che si è convertita in prodotto.
Si calcola con la seguente equazione:
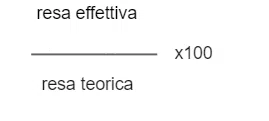
Cristina ha calcolato che la resa teorica di un esperimento è di 16,5 g di cloruro di sodio. Come risultato della reazione ha ottenuto 12,8 g di cloruro di sodio. Calcolare la resa percentuale dell'esperimento di Cristina.
resa effettiva / resa teorica x 100
(12.8 / 16.5) x 100
Resa percentuale = 77.576 %.
Cos'è la resa teorica?
La resa teorica (nota anche come resa prevista) è la quantità massima di prodotto che si può ottenere da una reazione.
La resa teorica è la resa che si otterrebbe se tutti i reagenti dell'esperimento si convertissero in prodotti.
Perché il rendimento effettivo è inferiore a quello teorico?
La resa effettiva è la quantità di prodotto che si ottiene effettivamente in un esperimento. È raro ottenere una resa del 100% in una reazione.
La resa effettiva è solitamente inferiore alla resa teorica per i seguenti motivi:
Alcuni dei reagenti non si convertono in prodotto.
Alcuni reagenti si disperdono nell'aria (se si tratta di un gas).
Le impurità bloccano la reazione.
Si producono sottoprodotti indesiderati in reazioni collaterali.
La reazione raggiunge l'equilibrio.
Equazione dei gas ideali
I gas hanno tre proprietà naturali: volume, pressione e temperatura. Gli scienziati sanno da tempo che esiste una relazione tra queste tre proprietà. La legge dei gas ideali è un'equazione che spiega la relazione tra le proprietà naturali dei gas. Ecco come si scrive l'equazione dei gas ideali:

P: pressione (Pa)
V: volume (m3)
n: numero di moli
R: costante dei gas
T: temperatura (K)
Calcolare il volume di 1 mole di un gas ideale a 0°C e alla pressione di 1 atmosfera.
0° = 273 K
1atm = 101325 Pa
R = 8.31441 JK-1mol-1
PV = nRT
101325 Pa x V = 1 mol x 8.31441 JK-1mol-1 x 273 K
V = 2269.83393101325
V = 0.0224 m3 o 22.4 dm3
Prima della legge dei gas ideali, gli scienziati avevano notato altre relazioni tra temperatura, pressione e volume dei gas.
Gli scienziati hanno scoperto che se la quantità di gas e la sua pressione rimangono invariate,
quando si cambia la temperatura, cambia anche il volume. Aumentando la temperatura
temperatura aumenta il volume. Abbassando la temperatura, il volume diminuisce.
Gli scienziati chiamarono questa scoperta Legge di Charles.
Hanno anche capito che il volume e la pressione sono inversamente proporzionali. Se il volume
aumenta, la pressione diminuisce. È vero anche il contrario! Questa relazione
è chiamata legge di Boyle.
Che cos'è un gas ideale?
I gas ideali si comportano secondo la teoria cinetica dei gas in tutte le condizioni di temperatura e pressione.
Ciò significa che le molecole di gas non hanno volume e non hanno forze attrattive tra loro. Se ci pensiamo bene, questo non può essere affatto vero! Quindi non esiste un gas ideale.
I gas che non obbediscono alla teoria cinetica dei gas sono chiamati gas reali.
Fortunatamente, la maggior parte dei gas reali si comporta in modo ideale.
Che cos'è la teoria cinetica dei gas?
La teoria cinetica dei gas spiega la relazione tra le proprietà di un gas. Descrive i gas come costituiti da minuscole particelle che non smettono mai di muoversi e che hanno molto spazio tra di loro.
Questa teoria si basa su alcuni concetti fondamentali.
I gas contengono molecole che si muovono in modo casuale in linee rette.
Le molecole di un gas si comportano come sfere rigide.
Quando le molecole di un gas collidono le pareti interne di un contenitore, esercitano una
certa pressione.
Quando le molecole si scontrano tra loro e contro il contenitore, non disperdono energia cinetica
(le collisioni sono completamente elastiche).
La temperatura del gas è correlata all'energia cinetica media delle sue molecole.
Le molecole hanno forze intermolecolari trascurabili tra loro.
Il volume occupato dalle molecole è trascurabile e relativo al volume del contenitore.
Quantità di sostanza - Punti chiave
- La mole (n) è l'unità SI per la quantità di sostanza. La quantità di entità elementari in una mole è pari al numero di atomi in 12 g dell'isotopo carbonio-12. Il numero di entità per mole è la costante di Avogadro. Il numero di entità per mole è la costante di Avogadro.
- L'equazione per il numero di moli è:
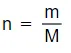
- La costante di Avogadro (L) è il numero di atomi presenti in 12 grammi di carbonio-12, ovvero 6.022 x 1023. Le diamo l'unità di misura mol-1, che si legge come "per mole".
- u è l'unità di misura della massa atomica. 1u equivale a 1/12 della massa di un atomo di carbonio-12. Tutti gli atomi vengono paragonati a 1/12 di carbonio-12 perché è uguale a 1u.
- La massa atomica relativa (Ar) è la massa media di tutti gli isotopi di un elemento, pesata per l'abbondanza di ciascun isotopo sulla Terra.
- La resa percentuale misura l'efficacia di una reazione chimica. Ci dice quanto dei nostri reagenti (in termini percentuali) si è trasformato in un prodotto.
- La formula per la resa percentuale è: (resa effettiva/resa teorica) x 100
- La resa teorica (nota anche come resa prevista) è la quantità massima di prodotto che si può ottenere da una reazione.
- La resa effettiva è la quantità di prodotto che si ottiene effettivamente da un esperimento. È raro ottenere una resa del 100% in una reazione.
- La legge dei gas ideali è un'equazione che spiega la relazione tra le proprietà naturali dei gas.
- L'equazione dei gas ideali è: PV = nRT.
- I gas ideali si comportano secondo la teoria cinetica dei gas in tutte le condizioni di temperatura e pressione.
- I gas che non obbediscono alla teoria cinetica dei gas sono chiamati gas reali.
- La teoria cinetica spiega la relazione tra le proprietà di un gas. Si basa sull'ipotesi che le molecole abbiano forze intermolecolari trascurabili tra loro e che il volume occupato dalle molecole sia trascurabile e relativo al volume del contenitore.