La cromatografia è una tecnica di separazione e di analisi utilizzata per separare una miscela solubile nei suoi componenti.
- Questo articolo tratta della cromatografia in chimica.
- Faremo una breve introduzione sulla cromatografia, immergendoci nella sua storia prima di esplorare i principi fondamentali.
- In seguito, esamineremo più da vicino i diversi tipi di cromatografia.
- Infine, discuteremo le diverse applicazioni ed utilizzi della cromatografia.
Che cos'è la cromatografia?
Supponiamo di avere un inchiostro viola intenso. Sebbene possa sembrare che contenga un solo colore, con la cromatografia possiamo dividerlo in tutti i suoi diversi pigmenti: blu, rossi, forse alcuni gialli e verdi. Questo è solo un esempio di cromatografia ed in questo caso, viene utilizzata per separare una miscela. Tuttavia, la cromatografia può essere utilizzata anche per analizzare le miscele, ad esempio per identificare i principi attivi di un farmaco e/o i prodotti di una reazione.
Il metodo della cromatografia
Esistono diversi tipi di cromatografia ed ogni tipo è caratterizzato da un processo leggermente diverso. Tuttavia, il metodo generale rimane lo stesso. La cromatografia prevede le seguenti fasi:
- Prendere una miscela solubile, nota come soluto.
- Aggiungere una piccola quantità di soluto a un mezzo statico solido, liquido o gassoso. Questo mezzo statico è noto come fase stazionaria.
- Aggiungere un solvente. Questa fase è nota come fase mobile.
- Il solvente è in grado di sciogliere il soluto e di trasportarlo attraverso la fase stazionaria.
- I diversi componenti della miscela attraversano la fase stazionaria a velocità diverse. Per questo motivo, si separano in macchie o bande chiare e distinte, che possono essere visualizzate su un cromatogramma.
- I diversi componenti della miscela attraversano la fase stazionaria a velocità diverse. Per questo motivo, si separano in macchie o bande chiare e distinte, che possono essere visualizzate su un cromatogramma.
Una delle forme più semplici di cromatografia è la cromatografia su carta. È molto probabile che l'abbiate già vista in qualche esperiento a scuola. Ecco come si presenta il tipico setup per la cromatografia su carta:
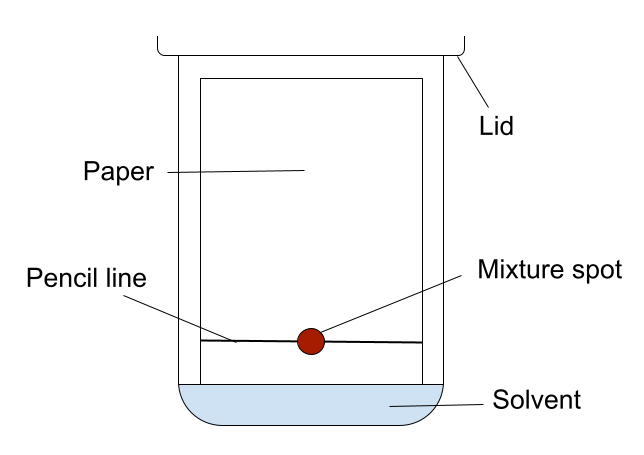
Figura 1. Tipico setup per la cromatografia su carta. StudySmarter Originals
La cromatografia fu inventata nel 1900 dal botanico italo-russo Mikhail Tsvet, che voleva separare i pigmenti dagli estratti vegetali. La parola cromatografia deriva dal greco chroma, che significa "colore", e graphein, che significa "scrivere". È interessante notare che anche il cognome di Tsvet significa "colore" in russo.
Questa tecnica, ha acquisito maggior importanza negli anni '40 e '50, in particolare grazie ad Archer Martin e Richard Synge, che hanno vinto il Premio Nobel per la Chimica nel 1952 per l'invenzione di un particolare tipo di cromatografia, nota come cromatografia di partizione.
Principi della cromatografia
In precedenza abbiamo introdotto alcune parole chiave, in particolare fase stazionaria, fase mobile e cromatogramma. Questi sono alcuni dei principi fondamentali della cromatografia. Ora analizziamo il loro significato.
Fase stazionaria
La fase stazionaria è un solido, un liquido o un gel statico. Il solvente trasporta la miscela solubile attraverso la fase stazionaria.
La fase stazionaria è, come suggerisce il nome stesso, ben ferma. Non si muove. Ne sono un esempio la carta e la polvere di silice.
Fase mobile
La fase mobile è il solvente utilizzato per trasportare la miscela analizzata attraverso la fase stazionaria.
A differenza della fase stazionaria, la fase mobile si muove. È un solvente che scioglie il soluto che si vuole analizzare o separare e lo trasporta attraverso la fase stazionaria.
Cromatogramma
Una volta terminata la cromatografia, la miscela si sarà separata sulla fase stazionaria in diverse macchie o bande. Il residuo della fase stazionaria, completo di tutte le macchie, è chiamato cromatogramma.
Un cromatogramma è una colonna o una striscia di materiale contenente componenti separati da una miscela mediante cromatografia. È essenzialmente il risultato di un esperimento di cromatografia.
Ad esempio, nella cromatografia su carta, la fase stazionaria è un foglio di carta. Una volta terminato l'esperimento, il cromatogramma è la carta con la disposizione finale dei diversi punti.
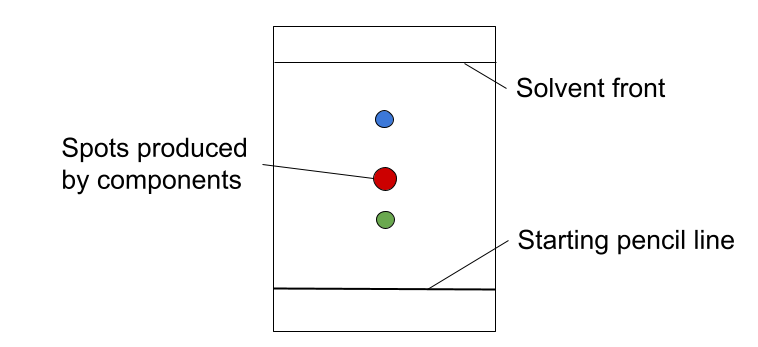
Figura 2. Un cromatogramma per la cromatografia su carta. StudySmarter Originals
Introdurremo successivamente la cromatografia su carta. Tuttavia, se non vuoi aspettare, dai un’occhiata a cromatografia su carta per maggiori dettagli.
Concentriamoci su due nuovi termini: affinità relativa e fattore di ritenzione.
Affinità relativa
I componenti della miscela si muovono a velocità diverse attraverso la fase stazionaria. Ciò dipende dalla loro affinità relativa alle due fasi.
In cromatografia, l'affinità relativa descrive la capacità di un componente di essere attratto dalla fase stazionaria o dalla fase mobile. Determina la velocità con cui il componente si muove attraverso la fase stazionaria.
Le componenti che presentano una maggiore attrazione per la fase stazionaria, hanno una maggiore affinità con la fase stazionaria. Sono quindi meno solubili nel solvente e sono più attratti dal mezzo statico. La fase mobile non può trasportarli con la stessa facilità: ciò significa che i componenti si muovono più lentamente attraverso la fase stazionaria.
Al contrario, le componenti che presentano una maggiore attrazione per la fase mobile, hanno una maggiore affinità con la fase mobile. Sono più solubili nel solvente e meno attratti dal mezzo statico. La fase mobile li trasporta facilmente, pertanto, queste componenti viaggiano più rapidamente attraverso la fase stazionaria.
A cosa sono dovute queste diverse affinità relative? Come abbiamo detto, tutto ha a che fare con l'attrazione per le due fasi.
Supponiamo che la fase stazionaria sia costituita da una molecola polare. Ciò significa che essa sperimenta forze dipolo-dipolo permanenti tra sé e gli altri componenti polari della miscela di partenza. D'altra parte, in genere si usa un solvente non polare. Ciò significa che ci saranno solo le forze deboli di Van der Waals tra il solvente e le componenti. Le componenti polari sono attratte più fortemente tra loro e la fase stazionaria, piuttosto che tra loro e la fase mobile. Essendo più attratte dalla fase stazionaria, e meno solubili nel solvente, possiamo affermare che hanno una maggiore affinità con la fase stazionaria.
Fattori di ritenzione
Ora sappiamo che le diverse componenti viaggiano a velocità diverse attraverso la fase stazionaria a causa della loro affinità relativa ai due stadi. Ciò significa che in un determinato periodo di tempo, ciascuna di esse, percorrerà distanze diverse. Questo fenomeno è facilmente visibile perché si presentano come macchie chiare e distinte.
Il rapporto tra la distanza percorsa da ciascun punto e la distanza totale percorsa dal solvente, viene utilizzata per calcolare il cosiddetto fattore di ritenzione o valore Rf.
I valori Rf sono importanti perché ci aiutano a identificare le componenti. Un particolare componente ha sempre lo stesso valore Rf in presenza di determinate condizioni, ovvero, se la temperatura, la fase mobile e la fase stazionaria sono esattamente gli stessi. Se calcoliamo il valore Rf di una particolare componente, possiamo confrontarlo con i valori presenti in un database per risalire all'identità di questa sostanza sconosciuta.
Per trovare i valori Rf, è necessario dividere la distanza percorsa da ciascun componente per la distanza totale percorsa dal solvente.

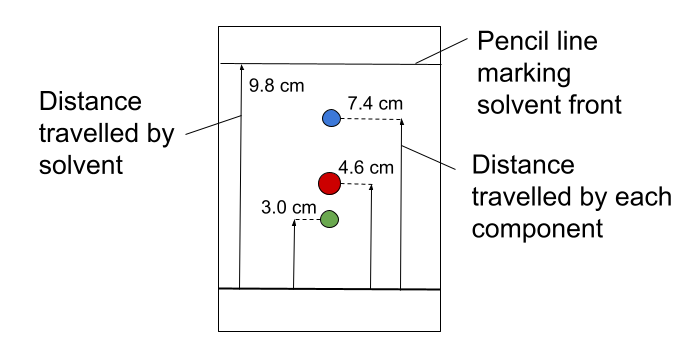
Figura 3. Calcolo dei valori Rf.StudySmarter Originals
Nell'esempio sopra riportato, la macchia blu ha percorso 7,4 cm e il solvente 9,8 cm. Per calcolare il valore Rf, si utilizza la seguente equazione:
I valori Rf non hanno unità e sono generalmente indicati con due cifre decimali.
Alcuni tipi di cromatografia utilizzano i tempi di ritenzione invece dei fattori di ritenzione. Questi misurano il tempo impiegato da ciascun componente per muoversi attraverso la fase stazionaria.
Ora che conosci le affinità relative, potresti prevedere come variano i valori di Rf tra le componenti?
- Le componenti con una maggiore affinità per la fase stazionaria viaggiano più lentamente attraverso il mezzo. Si muovono meno in un determinato periodo di tempo e quindi hanno un fattore di ritenzione più basso.
- Le componenti con una maggiore affinità per la fase mobile si muovono più rapidamente attraverso il mezzo. Si spostano più lontano in un determinato periodo di tempo e quindi hanno un fattore di ritenzione più elevato.
Tipi di cromatografia
Esistono diversi tipi di cromatografia. Si differenziano per le fasi mobili e stazionarie e per i metodi, ma tutti seguono i principi sopra descritti. Si distinguono in:
- Cromatografia su strato sottile (TLC).
- Cromatografia su carta.
- Gascromatografia.
- Cromatografia su colonna.
- Cromatografia di partizione.
- Cromatografia liquida ad alte prestazioni (HPLC).
E tante altre ancora.
Tabella riassuntiva per confrontare facilmente i diversi tipi di cromatografia.
| Nome | Fase stazionaria | Fase mobile | Note |
| TLC | Piatto ricoperto da un sottile strato di gel di silice | Solvente liquido | Accurata.Utilizzo di campioni piccoli. |
| Cromatografia su carta | Carta | Solvente liquido | Economica.Utilizzo di campioni piccoli. |
| Gascromatografia | Tubo riempito con polvere di silice | Solvente gassoso | Richiede calore.Estremamente sensibile. |
| Cromatografia su colonna | Colonna riempita con polvere di silice | Solvente liquido | Utilizzata principalmente per la separazione delle miscele. |
| Cromatografia di partizione | Colonna riempita di liquido su un supporto solido | Solvente liquido | La separazione avviene grazie alla diversa solubilità nelle due fasi. |
| HPLC | Colonna riempita con polvere di silice | Solvente liquido | Utilizza la pressione per accelerare il processo. |
Se desideri saperne di più su alcuni di questi tipi di cromatografia, dai un'occhiata ai nostri contenuti relativi alla cromatografia su strato sottile, alla cromatografia su colonna, alla gascromatografia, alla cromatografia su carta e alla cromatografia a scambio ionico.
Applicazioni della cromatografia
Abbiamo già parlato di alcuni usi della cromatografia come ad esempio, il suo utilizzo per l'analisi delle acque reflue. Tuttavia, ha un’ampia gamma di applicazioni diverse. Tra queste vi sono:
- Rilevazione di droghe nelle urine.
- Analisi dei metaboliti nei fluidi corporei.
- Estrazione di pigmenti da estratti vegetali.
- Isolamento dei principi attivi dei farmaci.
- Purificazione di composti.
- Separazione di miscele di proteine, aminoacidi o nucleotidi.
- Controllo di qualità delle bevande alcoliche
Ricordi lo scandalo della carne di cavallo del 2013? Si scoprì che alcuni prodotti a base di carne venduti come manzo contenevano in realtà carne di cavallo. Successivamente, gli scienziati sono riusciti a dimostrare l'origine della carne solamente frullandola e analizzandola con la cromatografia insieme a campioni di carne di cavallo pura.
Cromatografia - Punti chiave
- La cromatografia è una tecnica di separazione e di analisi utilizzata per separare una miscela solubile nelle sue parti componenti.
- La cromatografia prevede un mezzo statico, noto come fase stazionaria, un solvente, noto come fase mobile, e una miscela che si desidera analizzare. La fase mobile trasporta la miscela attraverso la fase stazionaria. Le diverse componenti della miscela hanno affinità diverse con ciascuna delle fasi e quindi si muovono a velocità diverse attraverso la fase stazionaria. Questo comporta la separazione.
- Un cromatogramma è una colonna o una striscia di materiale contenente le componenti che sono state separate da una miscela tramite la cromatografia. È essenzialmente il risultato di un esperimento con l’utilizzo della cromatografia.
- L'affinità relativa descrive la capacità di un componente di essere attratto dalla fase stazionaria o dalla fase mobile. Determina la velocità con cui il componente si muove attraverso la fase stazionaria.
- I fattori di ritenzione (valori Rf) indicano il rapporto tra la distanza percorsa da ciascun componente e quella percorsa dal solvente.
- Nelle stesse condizioni, lo stesso componente produce sempre lo stesso valore Rf.
- I tipi di cromatografia comprendono la TLC, la cromatografia su carta, la cromatografia su colonna, la gascromatografia, la cromatografia di partizione e l'HPLC.
- Alcuni usi della cromatografia comprendono la separazione di miscele, l'analisi delle acque reflue e l'isolamento dei principi attivi dei farmaci.