- Questo articolo tratta l'ossidazione degli alcoli.
- Inizieremo con i principi dell'ossidazione degli alcoli.
- Esploreremo l'ossidazione degli alcoli primari e vedremo il confronto con l'ossidazione degli alcoli secondari.
- Questo comporterà la comprensione dei reagenti, dei prodotti e delle condizioni necessarie per le reazioni.
- Considereremo anche l'ossidazione degli alcoli terziari ed esploreremo brevemente il meccanismo di ossidazione degli alcoli.
- Infine, vedremo come utilizzare l'ossidazione degli alcoli per verificare la presenza di aldeidi e chetoni.
Principi dell'ossidazione di alcoli
Forse sai già da Redox che l'ossidazione ha diverse definizioni:
- Addizione di ossigeno.
- Eliminazione di idrogeno.
- Perdita di elettroni che comporta un aumento dello stato di ossidazione.
Come si applicano queste definizioni alle reazioni di ossidazione degli alcoli? Iniziano ad avere un senso se consideriamo il carbonio alfa dell'alcol. Questo è l'atomo di carbonio che si unisce al gruppo idrossile -OH.
Quando gli alcoli vengono ossidati, il carbonio alfa subisce i seguenti cambiamenti:
- Forma un legame aggiuntivo con l'ossigeno.
- Perde un atomo di idrogeno.
- Aumenta lo stato di ossidazione.
Questa sembra un ossidazione!
Alla fine dell'articolo trovate un approfondimento sullo stato di ossidazione del carbonio alfa nei diversi calcoli e su come cambia nelle reazioni di ossidazione.
Reazione di ossidazione degli alcoli
Gli alcoli vengono ossidati tramite il riscaldamento in presenza di un agente ossidante. Tipicamente si utilizza il dicromato (Na2Cr2O7) di potassio(VI) . Per aumentare la velocità di reazione, acidifichiamo il dicromato di potassio utilizzando il catalizzatore acido solforico concentrato (H2SO4).
Tuttavia, non tutte le reazioni di ossidazione degli alcoli sono uguali. Le condizioni e i prodotti variano a seconda della classificazione dell'alcol. Vediamo di seguito:
- Gli alcoli primari (RCH2OH) vengono parzialmente ossidati ad aldeidi (RCHO) mediante distillazione. Possono poi essere ossidati completamente ad acidi carbossilici (RCOOH) con riflusso.
- Alcoli secondari (RCH(OH)R) sono ossidati a chetoni (RCOR) tramite il riflusso. Non possono essere ulteriormente ossidati.
- Gli alcoli terziari non possono essere ossidati.
Riassumeremo le definizioni di alcoli primari, secondari e terziari nel corso di questo articolo, ma se preferisci approfondire l'argomento, consulta Alcoli.
Ora che conosciamo le basi dell'ossidazione degli alcoli, possiamo esplorare più da vicino le diverse reazioni. Inizieremo con l'ossidazione degli alcoli primari.
Ossidazione degli alcoli primari
Ricordi la differenza tra alcoli primari, secondari e terziari? Dipende dal numero di gruppi R legati al carbonio alfa.
- Negli alcoli primari (indicati con il simbolo 1°), il carbonio alfa è legato a zero o a un solo gruppo R.
- Negli alcoli secondari (indicati con il simbolo 2°), il carbonio alfa è legato a due gruppi R.
- Negli alcoli terziari (indicati con il simbolo 3°), il carbonio alfa è legato a tre gruppi R.
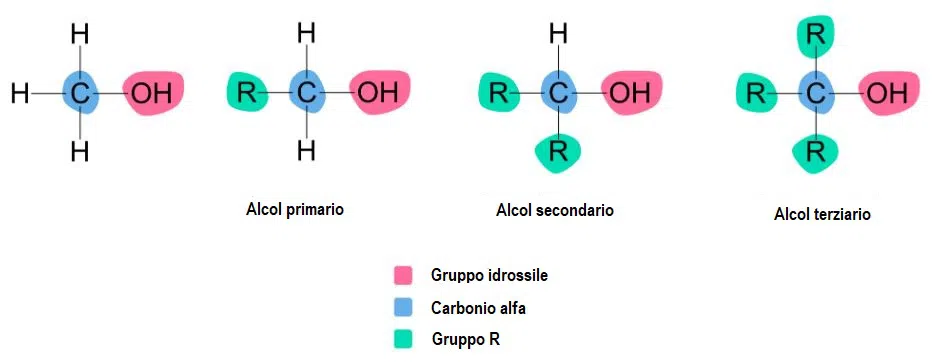
Figura 1. Alcoli primari, secondari e terziari con il carbonio in alfa, il gruppo idrossile ed i gruppi R evidenziati.
Gli alcoli primari hanno
due atomi di idrogeno attaccati al loro carbonio alfa (ad eccezione del metanolo (CH
3OH), che ne ha tre). All'inizio di questo articolo abbiamo scoperto che ogni reazione di ossidazione dell'alcol richiede che il carbonio alfa perda un atomo di idrogeno. Ciò significa che gli alcoli primari possono essere ossidati due volte: subiscono un'ossidazione sia
parziale che
completa.
Ossidazione parziale degli alcoli primari
Quando ossidiamo per la prima volta gli alcoli primari, li ossidiamo parzialmente. Come tutte le reazioni di ossidazione degli alcoli, si utilizza il dicromato di potassio(VI) acidificato con acido solforico concentrato. Tuttavia, per limitare l'ossidazione alla sola ossidazione parziale, si ricorre alla distillazione e a un eccesso di alcol. Si ottiene così un'aldeide (RCHO) e acqua (H2O).
Ecco l'equazione per l'ossidazione parziale degli alcoli primari. Si noti che abbiamo rappresentato l'agente ossidante usando [O], che è la notazione tipica delle reazioni di ossidazione.
RCH2OH + [O] → RCHO + H2O
 Figura 2. L'ossidazione parziale degli alcoli primari produce un'aldeide. I gruppi R e i gruppi funzionali delle due molecole sono evidenziati.
Figura 2. L'ossidazione parziale degli alcoli primari produce un'aldeide. I gruppi R e i gruppi funzionali delle due molecole sono evidenziati.
Confronta le due strutture qui sopra: l'alcol e l'aldeide. In generale, scambiamo il gruppo idrossile -OH dell'alcol con un doppio legame C=O (noto come gruppo carbonilico) e rimuoviamo un atomo di idrogeno dal carbonio alfa. Il carbonio alfa dell'alcol primario guadagna un ulteriore legame con l'ossigeno e perde idrogeno. Si ottiene così il caratteristico gruppo carbonilico -CHO dell'aldeide.
I gruppi funzionali non ti convincono? Non preoccuparti, abbiamo un articolo che fa al caso tuo! Dai un'occhiata ai Gruppi Funzionali per scoprire tutto quello che c'è da sapere sui diversi gruppi organici, sulle loro formule e sulle famiglie in cui si trovano.
Scrivi un'equazione per l'ossidazione parziale dell'etanolo. Indicare le condizioni della reazione e il nome del prodotto organico formato.
La parziale ossidazione dell'etanolo (CH3CH2OH) porta alla formazione dell'etanale (CH3CHO) e acqua. Utilizza la distillazione e un eccesso di alcol.
CH3CH2OH + [O] → CH3CHO + H2O
Ossidazione completa degli alcoli primari
Gli alcoli primari possono essere ossidati due volte e, osservando la struttura di un'aldeide, è facile capire come avviene. Le aldeidi contengono un atomo di idrogeno legato al carbonio alfa e quindi possono subire un'ulteriore ossidazione. Ancora una volta utilizziamo il dicromato di potassio acidificato, ma questa volta riscaldiamo la miscela a riflusso. La reazione produce un acido carbossilico (RCOOH). Si noti che quando si ossida un'aldeide non si produce acqua.
RCHO + [O] → RCOOH
 Figura 3. L'ossidazione di un'aldeide produce un acido carbossilico. I gruppi R e i gruppi funzionali della molecola sono evidenziati.
Figura 3. L'ossidazione di un'aldeide produce un acido carbossilico. I gruppi R e i gruppi funzionali della molecola sono evidenziati.
Confrontiamo ora l'aldeide e l'acido carbossilico. In questa seconda reazione di ossidazione, rimuoviamo l'atomo di idrogeno rimanente del carbonio alfa dell'aldeide e formiamo un ulteriore legame C-O al suo posto. L'idrogeno si unisce quindi all'altro lato del legame C-O, formando un gruppo ossidrile -OH. Nel complesso, il carbonio alfa dell'aldeide guadagna un legame con l'ossigeno e perde un atomo di idrogeno. Rimane il gruppo carbossilico -COOH degli acidi carbossilici.
È assolutamente possibile saltare il passaggio intermedio e passare direttamente da un alcol primario a un acido carbossilico ossidando l'alcol due volte in una solo passaggio. L'ossidazione di un alcol primario in questo modo è nota come ossidazione completa. Non ci preoccupiamo della distillazione, ma riscaldiamo semplicemente l'alcol a riflusso con un eccesso di dicromato di potassio(VI) acidificato. La reazione complessiva richiede due moli di agente ossidante per ogni mole di alcol e dà come risultato un acido carbossilico e acqua.
RCH2OH + 2[O] → RCOOH + H2O
Scrivi un'equazione per l'ossidazione completa dell'etanolo. Indicare le condizioni della reazione e il nome del prodotto organico formato.
L'ossidazione completa dell'etanolo (CH3CH2OH) produce acido etanoico (CH3COOH) e acqua. Si utilizza il riflusso e un eccesso di dicromato di potassio(VI) acidificato.
CH3CH2OH + 2[O] → CH3COOH + H2O
In breve, l'ossidazione parziale degli alcoli primari produce aldeidi, mentre l'ossidazione completa produce acidi carbossilici.
Metodo di ossidazione parziale e completa
Avrai notato le diverse condizioni richieste per l'ossidazione parziale e completa degli alcoli primari. Mentre l'ossidazione parziale richiede la distillazione e un eccesso di alcol, l'ossidazione completa richiede il riflusso e un eccesso di agente ossidante. Queste modifiche servono a controllare l'entità della reazione di ossidazione.
- Nell'ossidazione parziale, vogliamo ossidare l'alcol solo una volta e quindi manipolare le condizioni per evitare un'ulteriore ossidazione.
- Un eccesso di alcol significa che non c'è abbastanza agente ossidante per ossidare l'alcol una seconda volta.
- Le aldeidi hanno punti di ebollizione più bassi degli alcoli. L'uso della distillazione fa si che l'aldeide evapori non appena si forma, impedendo qualsiasi ulteriore reazione con l'agente ossidante.
- Nell'ossidazione completa, vogliamo ossidare l'alcol due volte e quindi manipolare le condizioni per garantire un'ulteriore ossidazione.
- L'uso di un eccesso di agente ossidante significa che l'agente ossidante è più che sufficiente per una seconda reazione di ossidazione.
- Il riflusso è una tecnica che fa sì che i vapori gassosi si condensino e ricadano nel recipiente di reazione. L'uso del riflusso impedisce all'aldeide formatasi nell'ossidazione parziale di evaporare e di uscire dal sistema. L'aldeide rimane invece intrappolata nel recipiente di reazione, dove può raggiungere temperature più elevate e reagire ulteriormente con l'agente ossidante.
Il diagramma seguente compara la tipica configurazione per l'ossidazione parziale e completa degli alcoli primari. Semplicemente cambiando le quantità relative dei reagenti e le condizioni di reazione, si può partire dagli stessi reagenti e ottenere due prodotti completamente diversi.
 Figura 4. A sinistra: set-up per la distillazione parziale. A destra: ossidazione completa a riflusso di alcoli primari Fonte: http://www.chembook.co.uk/
Figura 4. A sinistra: set-up per la distillazione parziale. A destra: ossidazione completa a riflusso di alcoli primari Fonte: http://www.chembook.co.uk/
Ossidazione di alcoli secondari
Gli alcoli secondari contengono due gruppi R attaccati al carbonio alfa C-OH. Questo li lascia con un solo atomo di idrogeno. Di conseguenza, gli alcoli secondari possono essere ossidati una sola volta. Gli alcoli secondari vengono ossidati riscaldandoli a riflusso con cromato di potassio acidificato, formando un chetone (RCOR) e acqua. L'uso di un eccesso di agente ossidante non fa differenza: i chetoni non possono essere ossidati ulteriormente!
L'equazione della reazione:
RCH(OH)R + [O] → RCOR + H2O
 Figura 5. Ossidazione degli alcoli secondari produce un chetone. Come in precedenza, i gruppi R ed i gruppi funzionali sono evidenziati.
Figura 5. Ossidazione degli alcoli secondari produce un chetone. Come in precedenza, i gruppi R ed i gruppi funzionali sono evidenziati.
Confronta le due strutture: l'alcol e il chetone. Scambiamo il gruppo idrossile -OH dell'alcol con un doppio legame C=O del gruppo carbonilico e rimuoviamo un atomo di idrogeno dal carbonio alfa. Nel complesso, il carbonio alfa dell'alcol secondario guadagna un legame in più con l'ossigeno e perde idrogeno. Si ottiene così il caratteristico gruppo carbonilico -CO- chetonico.
A differenza delle aldeidi, che possono essere ossidate nuovamente in acidi carbossilici, i chetoni non possono essere ulteriormente ossidati. Questo perché non ci sono legami C-H sul carbonio alfa del chetone e quindi l'ossidazione non può avvenire.
Scrivere un'equazione per l'ossidazione del propan-2-olo. Indicare le condizioni della reazione e il nome del prodotto organico formato.
L'ossidazione del propan-2-olo (CH3CH(OH)CH3) produce propanone (CH3COCH3) e acqua. Si utilizza dicromato di potassio acidificato e riflusso.
CH3CH(OH)CH3 + [O] → CH3COCH3 + H2O
Ossidazione di alcoli terziari
Gli alcoli terziari contengono tre gruppi R attaccati al carbonio alfa C-OH. Se si fa riferimento al diagramma riportato in precedenza nell'articolo, si può notare che ciò significa che il carbonio alfa non è legato ad alcun atomo di idrogeno - non ha legami C-H. Di conseguenza, gli alcoli terziari non possono essere ossidati. Il riscaldamento di un alcol terziario con dicromato di potassio (VI) acidificato non ha alcun effetto.
Perché non possiamo rompere, ad esempio, un legame C-C in una reazione di ossidazione? I legami C-C sono molto forti e stabili e la loro rottura richiede molta energia. Questo semplicemente non è favorevole alle reazioni di ossidazione.
Confronto ossidazione alcoli
Come riepilogo di tutto ciò che abbiamo imparato in questo articolo, abbiamo creato una tabella che riassume le reazioni di ossidazione degli alcoli primari, secondari e terziari.
| Tipo di ossidazione | Struttura alcol | Condizioni di reazione | Prodotto organico | Equazione |
| Alcol primario (ossidazione parziale) | RCH2OH | Distillazione, eccesso di alcol | Aldeide (RCHO) | RCH2OH + [O] → RCHO + H2O |
| Alcol primario (ossidazione completa) | RCH2OH | Riflusso, eccesso di agente ossidante | Acido Carbossilico (RCOOH) | RCH2OH + 2[O] → RCOOH + H2O |
| Alcol secondario | RCH(OH)R | Riflusso | Chetone (RCOR) | RCH(OH)R + [O] → RCOR + H2O |
| Alcol terziario | RC(OH)R2 | NA | NA | NA |
Abbiamo anche realizzato un diagramma per aiutarvi a visualizzare i prodotti delle reazioni di ossidazione degli alcoli e le loro strutture. Il diagramma evidenzia i gruppi R delle molecole e i loro diversi gruppi funzionali.
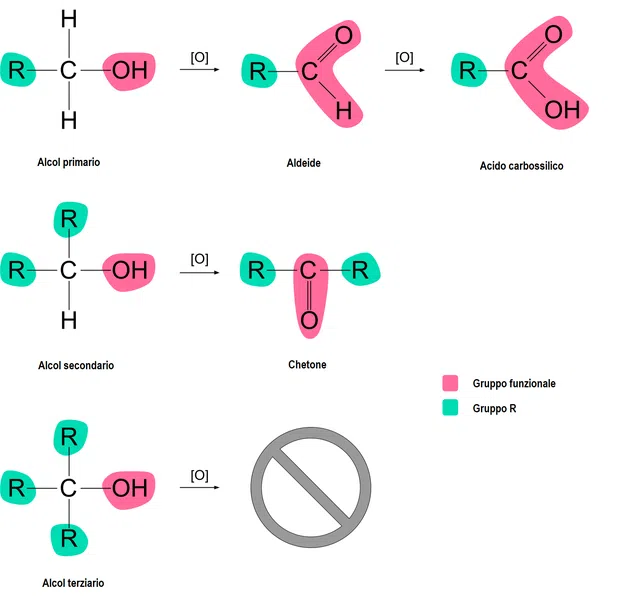
Figura 6. Le reazioni di ossidazione degli alcoli primari, secondari e terziari e i loro prodotti organici. Sono evidenziati i gruppi R e i gruppi funzionali delle molecole.
Meccanismo di ossidazione degli alcoli
L'ossidazione degli alcoli utilizza un meccanismo simile al meccanismo E2 visto nelle Reazioni di eliminazione degli alcoli. Si tratta essenzialmente di convertire il gruppo ossidrilico -OH in un miglior gruppo uscente, che viene poi eliminato dalla molecola. Tuttavia, questo meccanismo è estremamente complicato e per il momento concentrati semplicemente sulla comprensione dei reagenti, dei prodotti e delle condizioni per le diverse reazioni di ossidazione dell'alcol e sarete in grado di superare l'esame!
Stati di ossidazione nell'ossidazione degli alcoli
Ti ricordi che all'inizio dell'articolo abbiamo detto che l'ossidazione degli alcoli aumenta lo stato di ossidazione del carbonio alfa? Vediamo se questo è vero, calcolando lo stato di ossidazione del carbonio alfa in alcoli, aldeidi, acidi carbossilici e chetoni.
Forse non avete mai calcolato lo stato di ossidazione di uno specifico atomo di carbonio in una molecola organica. Ecco un semplice procedimento per iniziare.
- Scegli un atomo di carbonio.
- Comincia con lo stato di ossidazione +0.
- Considera ogni legame dell'atomo di carbonio con un altro atomo.
- Ogni legame con un atomo meno elettronegativo del carbonio diminuisce di 1 lo stato di ossidazione del carbonio.
- Ogni legame con un atomo più elettronegativo del carbonio aumenta di 1 lo stato di ossidazione del carbonio.
- I legami C-C non hanno alcun effetto sullo stato di ossidazione del carbonio.
- Sommando gli effetti di tutti i legami, si ottiene lo stato di ossidazione complessivo dell'atomo di carbonio.
Abbiamo calcolato lo stato di ossidazione degli atomi di carbonio alfa in diversi alcoli e i loro prodotti di ossidazione nel diagramma sottostante. Ricordiamo che un gruppo R è un'abbreviazione di un gruppo alchilico, e quindi conta come un legame C-C - non ha alcun effetto sullo stato di ossidazione del carbonio alfa.
 Figura 7. Stato di ossidazione del carbonio alfa negli alcoli primari, alcoli secondari, aldeidi, chetoni e acidi carbossilici. L'effetto di ciascun legame è mostrato nella figura.
Figura 7. Stato di ossidazione del carbonio alfa negli alcoli primari, alcoli secondari, aldeidi, chetoni e acidi carbossilici. L'effetto di ciascun legame è mostrato nella figura.
Ossidazione di alcoli: test per aldeidi e chetoni
Esistono un paio di applicazioni utili per l'ossidazione degli alcoli. Possiamo usare ciò che sappiamo sulle reazioni di ossidazione degli alcoli per testare la presenza di aldeidi e chetoni.
Ricordiamo che le aldeidi (prodotte dall'ossidazione di un alcol primario) possono essere ulteriormente ossidate, mentre i chetoni (prodotti dall'ossidazione di un alcol secondario) no. Molti agenti ossidanti, quando reagiscono, presentano un netto cambiamento di colore che ci permette di distinguere positivamente tra queste due famiglie. È necessario conoscere tre agenti ossidanti in particolare:
- Abbiamo già incontrato il dicromato di potassio (VI). Il dicromato di potassio (VI) è naturalmente di colore arancione, ma quando reagisce diventa verde.
- Un altro agente ossidante è il reattivo di Tollens. È naturalmente incolore, ma quando riesce a ossidare una specie forma un residuo di argento a specchio.
- Il terzo agente ossidante che potrebbe essere testato è la soluzione di Fehling. Se la soluzione blu forma un precipitato rosso scuro, si sa che è avvenuta una reazione di ossidazione.
 Figura 8. Cambiamento di colore degli agenti ossidanti quando riescono ad ossidare un'altra specie.
Figura 8. Cambiamento di colore degli agenti ossidanti quando riescono ad ossidare un'altra specie.
Per distinguere tra aldeidi e chetoni, è sufficiente riscaldarli delicatamente con uno degli agenti ossidanti sopra riportati. La tabella seguente riassume i cambiamenti di colore che ci si aspetta di vedere.
| Specie | Osservazione con dicromato di potassio | Osservazione con reattivo di Tollens | Osservazione con soluzione di Fehling |
| Aldeide | Soluzione verde diventa arancione | La soluzione incolore forma un residuo d'argento a specchio | La soluzione blu forma un precipitato rosso scuro |
| Chetone | La soluzione rimane verde (nessuna reazione visibile) | La soluzione rimane incolore (nessuna reazione visibile) | La soluzione rimane blu (nessuna reazione visibile) |
Si noti che possiamo usare il reattivo di Tollens e la soluzione di Fehling solo per ossidare le aldeidi in acidi carbossilici. Non possiamo usarli per ossidare gli alcoli primari o secondari rispettivamente in aldeidi o chetoni. L'ossidazione diretta degli alcoli richiede un forte agente ossidante e il reattivo di Tollens e la soluzione di Fehling sono entrambi troppo deboli. Tuttavia, il dicromato di potassio acidificato è adatto allo scopo!
Ossidazione di alcoli - Punti chiave
- Gli Alcoli partecipano a reazioni di ossidazione. Queste introducono un ulteriore legame C-O nella molecola e rimuovono l'idrogeno.
- Per ossidare un alcol, lo riscaldiamo con un agente ossidante. In genere si usa il dicromato di potassio (VI) (Na2Cr2O7) e un catalizzatore di acido solforico concentrato (H2SO4).
- Le reazioni di ossidazione degli alcoli variano a seconda della struttura dell'alcol.
- Gli alcoli primari vengono parzialmente ossidati in aldeidi utilizzando la distillazione e un eccesso di alcol.
- Gli alcoli primari possono anche essere completamente ossidati in acidi carbossilici utilizzando il riflusso e un eccesso di agente ossidante.
- Gli alcoli secondari vengono ossidati in chetoni mediante riflusso.
- Gli alcoli terziari non possono essere ossidati.
- I principi alla base dell'ossidazione dell'alcol ci permettono di analizzare sostanze organiche specifiche. Le aldeidi possono essere ulteriormente ossidate da agenti ossidanti, mentre i chetoni no. Riscaldando il dicromato di potassio(VI), il reattivo di Tollens o la soluzione di Fehling, che sono tutti esempi di agenti ossidanti, con un'aldeide si ottiene un netto cambiamento di colore. Tuttavia, riscaldandoli con un chetone non si ottiene alcuna reazione visibile.